- ナースが知っておきたい栄養の基本と栄養サポートの進め方 >
- Part1 栄養の基礎 >
- 4.体液の分布と浸透圧
ナースが知っておきたい 栄養の基本と栄養サポートの進め方
著・若草第一病院 院長 山中英治
2019年1月公開
Part1 栄養の基礎
4.体液の分布と浸透圧
1) 細胞内液と細胞外液
体重の60%は水分です。水分のうち体重の40%は細胞内液で、体重の20%が細胞外液です。細胞外液のうち体重の15%が(細胞)間質液で、体重の5%が血管内液(血漿)です(図12)。
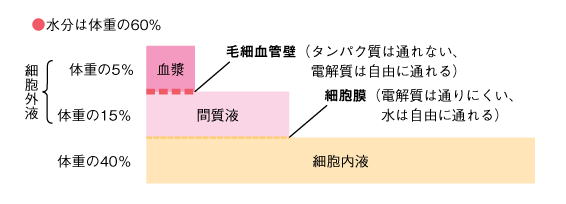
輸液は血管(静脈)内に液体を入れます。静脈内に入った液体は心臓から全身にまわり毛細血管から身体中に分布します。輸液の成分によって細胞外液や細胞内液への分布の仕方が異なります。
2) 細胞内外の水分移動
細胞内外の水分移動には、(晶質)浸透圧が関与します。(晶質)浸透圧は、半透膜(例えば細胞膜)で隔てられた濃度の異なる2液間で、濃度の低いほうから高いほうへ移動する圧力です。電解質、糖質、アミノ酸のような溶質(水などの溶媒に溶けている物質)によって生じます。
浸透圧は、溶液中の粒子の数、すなわち溶媒の容量(L)中の溶質の粒子数で表します。粒子数の単位はモル(mol)で、粒子が6.02×1023個集まった単位が1molです。浸透圧は粒子の数mol÷溶質の容量(L)で、浸透圧の単位はオスモル濃度Osm/Lで表します。ちなみに、1mol集まった分子の質量(g)が分子量です。
ヒトの血漿浸透圧は285±5mOsm/Lであり、浸透圧は細胞内外で等しくなるように平衡状態が保たれています。mOsmはOsmの1/1000の単位です。
電解質は、溶液のなかでイオン分解して、陽イオンと陰イオンに分かれます。+または-の電気を帯びたイオンに分かれるので、電離といいます。例えば、塩化ナトリウム(食塩)は水に溶かすと、Naイオン(Na+)とClイオン(Cl-)に1:1に電離します。すなわち、完全にNa+とCl-に分かれると、合わせた粒子数は、溶ける前のNaClの粒子数の倍になります。一方、ブドウ糖のように、水に溶かしても電離しない物質を、非電解質といいます。
電子1個分のはたらきをするものを1価のイオン、2個分のはたらきをするものを2価のイオンといいます。+の電気を帯びたイオンを陽イオン、-の電気を帯びたイオンを陰イオンといいます(表8)。
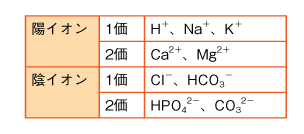
輸液製剤に記載されている電解質の濃度の単位に、mEq/L(ミリイクイヴァレント/リットル)(ミリ当量)があります。Eqは「当量」と訳されます。Eq/Lは当量濃度で、溶液1Lに溶けている電解質の当量です。mEqはEqの1/1000の単位です。
非電解質は電離しないので、価数は無関係です。そのため、含まれる溶質の重量(g)やg/L濃度、溶液1Lに溶けている溶質のモル数のモル濃度(mol/L)=Osmなどで記載されることが多いです。 電解質は電離して粒子の数が増えるのに加えて、電荷の価数が陽イオンと陰イオンの数のバランスに影響します。そこで、価数も計算に入れたほうがバランスがわかりやすいので、電解質の濃度は当量濃度で記載されています。電解質の当量濃度(Eq/L)は、「電離した粒子の価数の合計÷溶液の容量」になります。
なお、浸透圧は価数ではなく粒子数で決まるので、電解質においても浸透圧の単位はmOsm/Lです。
細胞内と細胞外では、多く含まれる電解質が異なります。細胞内液に最多の陽イオンはK+で、細胞外液に最も多いのはNa+です。血漿も細胞外液なので、血漿浸透圧に最も影響する電解質はNa+です。Na+が細胞外液の浸透圧、水を引っ張る力を左右しているのです。
血漿浸透圧:2×血清Na(mEq/L)+(血糖[mg/dL]÷18)
*
以上のように、電解質は電離してイオンバランスや浸透圧に影響するので、血液検査の血清電解質のNa、K、Clの測定値の単位はmEq/Lです。ただし、測定装置の関係で、Ca、Mg、Pはmg/dLで表記されていることもあるので、基準値に注意してください。
3) 血管内外の水分移動
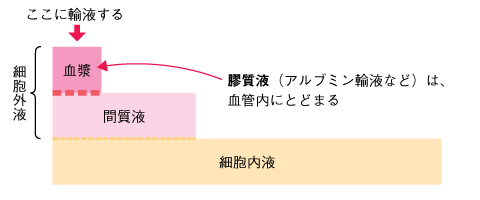
毛細血管の血管壁には、電解質は通しますが、アルブミンなどの血漿タンパクは通さない「バリア」があります。血管内液も血管外液も、どちらも細胞外液ですが、この「バリア」のおかげで血管内のほうが濃度勾配が高くなります。そのため、血管内に水を引っ張って、血管内水分量を維持できるのです。
この血漿タンパクによる力を、膠質浸透圧といいます。膠質とは、コロイドのことです。膠質輸液には、アルブミン液や代用血漿製剤(デンプンを主成分としたコロイド輸液など)があります。急な出血などで血管内水分が失われて血圧が維持できないときには、循環血液量を補い、ショック状態から離脱する目的で、膠質輸液が投与されます。
低分子物質(電解質、糖質、アミノ酸)によって細胞膜を介して生じる晶質浸透圧と、高分子物質(血漿タンパク)によって血管壁を介して生じる膠質浸透圧を混同しないようにしましょう(表9、図13)。
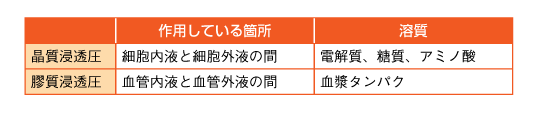
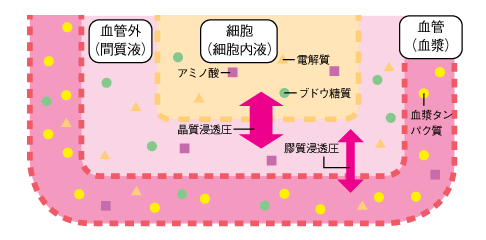
矢吹浩子編:ナースのために ナースが書いた ココが知りたい栄養ケア.照林社,東京,2016:81.を元に作成
4) 生理食塩水と5%ブドウ糖液
輸液の浸透圧は、配合されている電解質、糖質、アミノ酸などの濃度によって異なります。体液の浸透圧(285±5mOsm/L)と等しい(晶質)浸透圧の輸液を等張液、低い輸液を低張液、高い輸液を高張液といいます。
低張液としては、粒子を含まない、つまり浸透圧0の蒸留水があります。これを大量に投与すると、赤血球の細胞膜を介して浸透圧で水が赤血球内に充満し、赤血球が壊れて(溶血)しまいます。そのため、蒸留水単独の静脈内輸液は禁忌です。
高張液としては10%塩化ナトリウム(NaCl)液などがあります。このような高浸透圧の液を急速に投与して、急に血中Na濃度が上昇すると、細胞内水分が浸透圧で引き出され、細胞内脱水により浸透圧性脱水症候群が起こります。そのため、低Na血症の補正の際などには、注意が必要です。
等張輸液の代表として、生理食塩水と5%ブドウ糖液があります。
①生理(的)食塩水
生理(的)食塩水は、血漿浸透圧に近いので生理的と表現されています。食塩(塩化ナトリウム、NaCl)9gを水に溶かして、1Lに調整します。9g/Lとなるので、濃度は0.9%です。
NaClの分子量は、Na(分子量23)+Cl(分子量35.5)=58.5です。NaClが1モル(mol)あると、質量は58.5gになります。生理食塩水1L(1000mL)中にはNaClが9g溶解しているので、9(g)÷58.5=0.154mol/1000mLです。つまり、生理食塩水(NaCl)のモル濃度は、154mmol/L(154mOsm)となります。
NaClは、水に溶けるとNa+とCl-の粒子(イオン)に電離します。浸透圧は、溶液内の粒子の数に比例します。Na+とCl-が、1Lの溶液内にそれぞれ154mmolずつ存在するので、浸透圧は154+154=308mOsm/Lになります。実際には、NaClは100%電離せずに、約85%が電離して残りはNaClのままで存在します。そのため、生理食塩水を浸透圧計で実測すると、測定値は285mOsm/Lになります。これは、血漿浸透圧と等しい値です。生理食塩水の電解質であるNa+とCl-は、どちらも1価のイオンなので、当量濃度はいずれも154mEq/Lになります。
②5%ブドウ糖液
5%ブドウ糖液の浸透圧も血漿浸透圧に近いので、電解質を入れずに水分のみを補充したいときによく用いられます。ブドウ糖は非電解質なので電離しません。ブドウ糖50gを1Lの水に溶かすと、濃度は50g/Lで5%になります。ブドウ糖は分子式C6H12O6なので、分子量は以下のように計算できます。
C(分子量12)×6個=72
H(分子量1)×12個=12
O(分子量16)×6個=96 72+12+96=180
ブドウ糖の分子量は180、つまり1molは180gです。5%ブドウ糖液のモル濃度は、50(g)÷180=0.278mol/1000mL、つまり278mmol/Lとなります。
ブドウ糖は電離しないので、水に溶かしても粒子数は変わりません。そのため、浸透圧は278mOsm/Lで、血漿浸透圧に近い値になります。
*
生理食塩水と5%ブドウ糖液は、どちらも粒子数では等張液ですが、体内での分布の仕方が異なります。
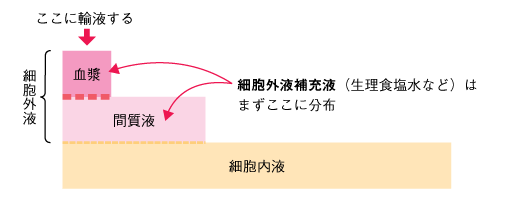
生理食塩水の電解質組成は細胞外液に似ているので、生理食塩水を投与すると、細胞外液(血管内と細胞間質)に分布します。
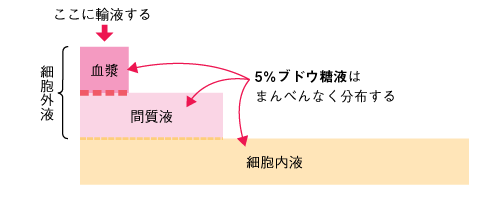
一方、ブドウ糖液は電解質を含まないので、血管内や間質に長くはとどまりません。5%ブドウ糖液を投与すると、ブドウ糖は速やかに体内に吸収されるため、水分のみを補給することになり、血管内から容易に細胞間質を経て細胞内液にもまんべんなく水分が分布します。
主な輸液の分類と分布を図表に示します(表10、図14)。

■細胞外補充液の分布
ログイン
「ディアケア」に
会員登録(無料)すると
できること
限定コンテンツ
実践のコツや記事などの
「限定コンテンツ」が見られる!
資料ダウンロード(PDF)
一部の記事で勉強会や
説明など便利に使える資料を公開中!
ケア情報メール
新たなコンテンツの
公開情報や、ケアに役立つ情報をお届け!
【有料サービス】「ディアケア プレミアム」に
登録するとできること(月額800円~/無料お試しあり/法人利用も可能)
実践ケア動画
エキスパートのワザやコツが
学べる動画を多数掲載!
期間限定セミナー動画
各分野のエキスパートが登壇。
1回約15分で学べる!
電子書籍
書店で販売されている本や、
オリジナル書籍が読み放題!



